|
一、相关律例 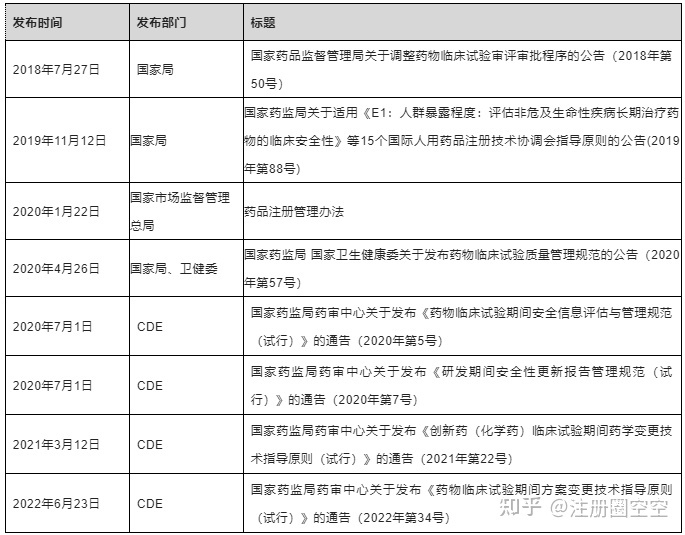             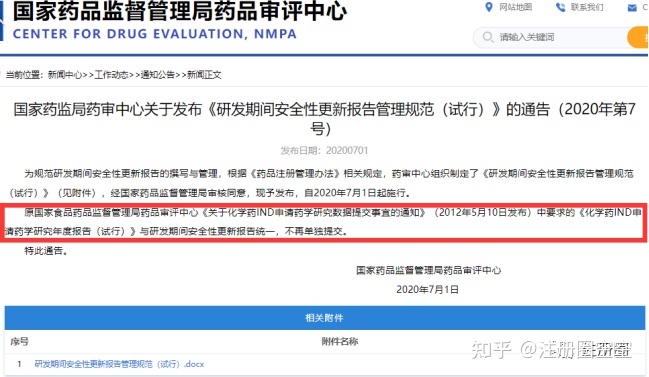       1、目标 DSUR的首要目标是药品注册申请人(以下简称申请人,也包括申办者)对报告周期内收集到的与药物(不管上市与否)*相关的平安性信息停止周全深入的年度回首和评价。 *处于研发阶段的药物(包括已上市但仍在进一步研讨的药物)。 2、根基原则 1)依照ICHE2F指导原则的要求预备、撰写和提交DSUR。2)预备和递交DSUR的义务
3)DSUR需要包括与一切剂型和规格、一切顺应症以及研讨中接管研讨药物的患者人群相关的数据(化学药依照不异活性成份)。假如相关信息没法获得(如申请人尚未获得数据),申请人应在DSUR的前言部分予以诠释说明。4)申请人获批后均应向CDE提交DSUR。5)DSUR原则上应将药物临床实验在境内大概全球初次获得临床实验答应日期(即“国际研发诞生日”:DIBD)的月和日,作为年度报告周期的肇端日期。初次提交应在境内临床实验获准展开后第一个DIBD后两个月内完成,后续提交也应以DIBD为基准。举例以下:  6)DSUR应延续提交至该药物境内最初一个上市答应申请提交,大概在境内不再继续停止研发时为止。最初一次提交时应附说明文件,说明该次提交为在境内的最初一份DSUR,并说明申请人能否还在其他国家大概地域继续停止临床实验。(举例:本次提交为国内最初一份DSUR,我司仍在美国继续停止临床实验)7)当药物在境内外获得了上市答应,如申请人需要,可以在全球首个获得上市核准日期(即“国际诞生日”,以下简称IBD)的根本上预备和提交DSUR。调剂后的初次提交,报告周期不应跨越一年。举例以下:  3)撰写要求 1)DSUR全文及附件   2)支持性材料:报告周期内申请人以为不影响受试者平安的药物临床实验计划变更大概临床方面的新发现、非临床大概药学的变化大概新发现的支持性材料。3)若有。申请人还应视情况(如最初一次提交DSUR),随DSUR提交需要的说明性文件。(举例:本次提交为国内最初一份DSUR,我司仍在美国继续停止临床实验) 4)提交    注:1.申请人可以授权第三方停止DSUR的提交。 2.文件上传(均为pdf文件)包括以下内容: (1)DSUR报告; (2)研讨者手册(IB) (3)地区性附件1-5 (4)支持性材料 在预备DSUR报告时,可以先预备一份完整的DSUR(包括研讨者手册和地区性附件,在上传材料前再停止拆分)。 三、DSUR具体内容 封面、履行提要、目录、章节1-20以及附件。具体拜见ICH E2F指导原则及其示例。ICH E2F指导原则及其示例可以在CDE网站“ICH工作办公室专栏”下载。   其中第16节“地区特有信息”应合适国家或地域要求。国内要求的地区附件1-5以下所示(来历于《研发时代平安性更新报告治理标准(试行)》):  E2F DSUR 示例以下:   E2F DSUR 示例以下: 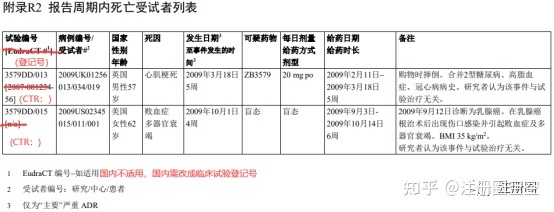  E2F DSUR 示例以下:  附件 4 报告周期内发生的药物临床实验计划变更大概临床方面的新发现、非临床大概药学的变化大概新发现总结表 申请人应以列表形式,对报告周期内发生的药物临床实验计划变更、非临床大概药学的变化大概新发现停止总结,示例拜见附表1。 对于能够增加受试者平安性风险的,申请人应依照药学的变化大概新发现、非临床的变化大概新发现、药物临床实验计划变更大概临床方面的新发现三各种别,总结已提交的补充申请的受理号、申请事项、承办日期及能否获批(是/否/在审)。不需供给支持性材料。 对于申请人评价以为不影响受试者平安的,申请人应依照药学的变化大概新发现、非临床的变化大概新发现、药物临床实验计划变更大概临床方面的新发现三各种别,总结其内容、时候、种别,并说明对应支持性材料的申报材料项目编号大概人用药物注册申请通用技术文档(以下简称CTD)中的模块及章节编号。申请人应参照化学药、生物制品和中药注册分类及申报材料要求、CTD等要求,预备响应的支持性材料与DSUR一并提交。对于报告周期内已提交过的相关材料(如用于相同交换的材料,因展开后续分期药物临床实验,已在药品审评中心网站提交的药物临床实验计划和支持性材料),应在备注栏中说明提交路子、时候和参考编号(如相同交换申请编号等),不需反复提交。 举例以下:   注:对于上传到CDE的支持性材料,如药学研讨材料3.2.P.5,是需要拆分到二级目录的,即拆分红3.2.P.5.1、3.2.P.5.2、3.2.P.5.3、3.2.P.5.4....是以需要预备好拆分支持性材料的时候,大概撰写时依照二级目录撰写每个材料。 附件 5 下一报告周期内整体研讨计划提要 申请人应简要供给以下内容:一、下一报告周期内临床研讨整体计划提要(一)立题根据;申请人应简要描写下一报告周期内计划停止的临床实验的立题根据。(二)拟研讨的顺应症;申请人应列出下一报告周期内,计划停止研讨的未上市顺应症。(三)评价药物时所遵守的整体途径;简要描写下一报告周期内,计划展开临床实验的顺序大概对计划研讨的患者人群停止简要描写。(四)下一个报告周期内拟展开的临床实验;简要描写下一报告周期内,计划展开的临床实验的实验设想(假如没有制定全年的计划,申请人应予以说明)。(五)估计受试者人数;下一报告周期内计划展开的临床实验中,估量的受试者人数;(六)估计的风险。基于动物的毒理学大概既往人用实验的数据,估计的任何与药物大概相关药物有关的严重大概重度风险。 二、下一报告周期内非临床研讨整体计划提要简要描写下一报告周期内计划新展开大概继续停止的非临床研讨。 三、下一报告周期内药学研讨整体计划提要简要描写下一报告周期内计划新展开大概继续停止的药学研讨。最初,撰写DSUR时需要药物鉴戒、药学、医学、临床、非临床和注册等部分相互配合,预留充足的时候停止撰写、订正、定稿、签批及上传。 经历有限,有误之处可联系注册圈治理员停止更正。 |

很早以前写的培训用的Makefile文档,整理好分享给大家。本文用Linux服务器下编写C程序

有一个有趣的段子说,不同阶段的学生写论文就如同打兔子:本科生是老师告诉你死兔子在
完全可行的副业,每年多赚20万不是问题!我自己做过很多副业,从头条号、公众号、淘宝

一、砂锅的历史二、砂锅的材质分类三、砂锅的器型分类四、砂锅的著名产地五、为什么砂

这篇文章大概发了一个月左右的时间,承蒙大家厚爱,收到了许多赞和评论。大家问的最多

被骗怎么办。答案是维权!!一下是我的维权过程。可能有点长。但比较详细。想看干货直接
大家好!我是喜欢把问题研究明白的调皮哥,感谢关注我。我创建了一个【雷达工程技术交

作者:cherry it up(来自豆瓣,点击可阅读原文“中立” “客观” “理性”的迷思)今
前言最近可能很多使用 Chrome 的用户都发现了,Chrome 浏览器右键菜单里的网页翻译失
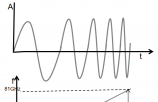
大家好,我是 @调皮连续波 ,江湖人称“调皮哥”。正值五一假期,去哪里都人多,因此
首先,这里需要申明的一点!解决国内如何使用TikTok真的非常简单,没有大家及网上说的
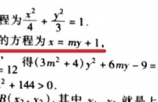
破300赞 更新一下首先统一回复一下质疑最多的问题明明都是学校讲过得啊,简单的变形而
各位老少爷们儿,这好像是我第一次在知乎写文章!不一定能有多少人看的到,尤其是针对

【一】干货较多,希望兄弟们耐心看完。这一期讲的主要是这四个东西中的跟风。后面还会
渗透测试,是专业安全人员为找出系统中的漏洞而进行的操作。当然,是在恶意黑客找到这

有没有同感,一来到广州就懵了啊!广州好吃的、好看的实在是太多了!想买个特产,都不
{color{red}{看完这篇,再也不用为英语语法发愁啦(保真) !}} 这篇文章可以在 15

【本文章推荐实习信息——腾讯视频VIP商务合作渠道拓展】岗位信息在文末哦~欢迎关注,

C语言是当代人学习及生活中的必备基础知识,应用十分广泛,下面为大家带来C语言基础知
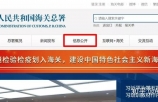
海关统计数据在线查询系统优化升级了,系统更好用啦!1.进入海关总署官网http://www.c
声明:本站内容由网友分享或转载自互联网公开发布的内容,如有侵权请反馈到邮箱 1415941@qq.com,我们会在3个工作日内删除,加急删除请添加站长微信:15924191378
Copyright @ 2022-2024 私域运营网 https://www.yunliebian.com/siyu/ Powered by Discuz! 浙ICP备19021937号-4