|
波尔氢原子模子根本常识 上一期,跟小伙伴们讲授了光电效应,没想到结果很理想,小伙伴赐与很多积极评价,感激小伙伴们的支持。所以,这一期,我们再讲一个根本的常识点。波尔氢原子模子! 波尔的氢原子模子也很好了解,可是很多小伙伴对其中一些最最最根基概念还是存在一些模糊的熟悉,我们只管讲得具体一些。 先说为什么是氢原子模子呢?由于最简单,只要原子核和一个核外电子。以下图,意味性地画一个氢原子。核外电子(带负电)绕着原子核(带正电)作圆周活动。  究竟上,对于稍微复杂一点点的,如氦原子,波尔理论实在就没法诠氏缢。所以,我们高中阶段讲波尔原子理论,也就只讲氢原子了。 【能量】首先,我们说一说氢原子的能量。氢原子的能量由核外电子的动能、电子与原子核势能两部分组成。 氢原子总能量=核外电子动能+原子势能。 【留意】动能是核外电子的,势能是电子和原子核系统的。 【鉴戒】小伙伴们可以鉴戒外有引力章节的行星模子,获得: 当核外电子离原子核越远时,电子动能越小,原子势能越大,总能量也越大! 是以,原子的能量与核外电子与原子核的间隔具有对应关系! 这点很重要,小伙伴可以从电场力做功等角度去了解。 【量子化轨道】量子化简单了解为不持续性,普朗克提出量子概念后,爱因斯坦将其应用于光电效应,波尔将其应用于原子模子中。量子化轨道是说,原子核外电子绕核活动的轨道是不持续的。 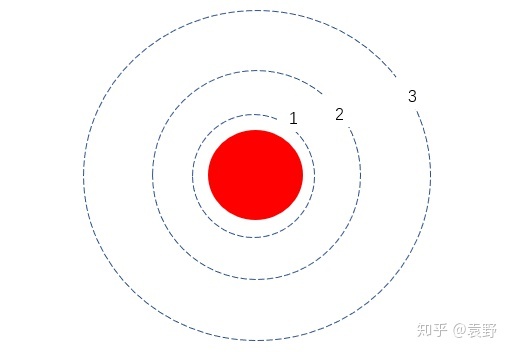 如上图所示,1,2,3为电子活动的能够轨道,但1,2,3之间没有其他轨道,电子会像“鬼魂”一样间接从1轨道到2轨道。各能够轨道满足以下关系:
其中 【量子化能量-能级】由于核外电子的轨道不持续,是以,按照: 氢原子总能量=核外电子动能+原子势能 氢原子的能量也不持续的,称为能级,各能级之间的关系满足:
由于能量为负数,所以能级越高能量越大! 当
按照公式可以计较其他各态,称为激起态的能量:
当 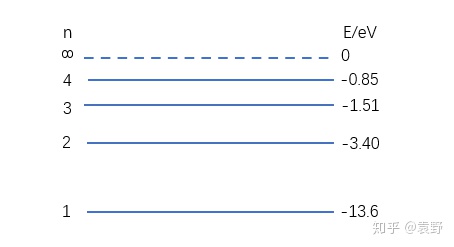 【能级跃迁1-光子吸收】接下来,我们讲跃迁,跃迁可以有两种了解,一种是电子轨道跃迁,一种是原子能级跃迁,实在这两种是对应的(轨道变化陪伴着能量变化),我们一般讲原子能级跃迁。 低能级的原子需要经过吸收光子来获得能量,从而向高能级跃迁,比如: 一个处于第2能级(-3,40eV)的氢原子吸收了一个能量为1.89eV的光子后就能跃迁到第3能级(-1.51eV)。 可是一个处于第2能级(-3,40eV)的氢原子面临一个比如能量为2.00eV的光子,将力所不及,由于吸收后没有响应的能级可以到达! 【思考1:实物粒子碰撞】上面说了,对于能级跃迁进程中吸收光子的情况,只能恰好吸收某些特别能量的光子。可是从低能级向高能级跃迁还有一种方式,就是用实物粒子撞击。比如:用能量为2.00eV的自在电子撞击处于第2能级氢原子(-3.40eV),则氢原子可以吸收自在电子1.89eV的能量跃迁到第3能级(-1.51eV),自在电子在促使氢原子跃迁后还残剩0.11eV能量。 【能级跃迁2-光子发射】相反,原子从高能级向低能级跃迁时,会发出光子,比如从第3能级向第2能级跃迁时会放出1.89eV能量的光子。 【思考1:一个和一群】比如一个处于第4能级的氢原子,它向低能级跃迁有哪些情况呢? 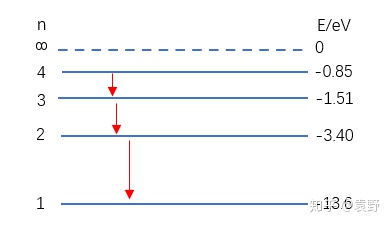 第一种情况,如上图,从第4能级跃迁到第3能级,再从第3能级跃迁到第2能级,再从第2能级跃迁到第1能级。是以可以放出3种分歧能量的光子。 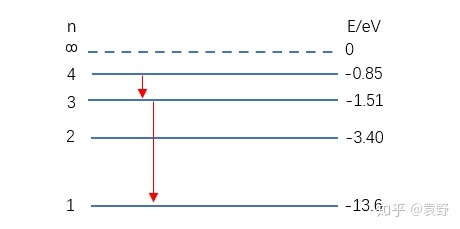 第二种情况,如上图,从第4能级跃迁到第3能级,再从第3能级间接跃迁到第1能级。是以可以放出2种分歧能量的光子。 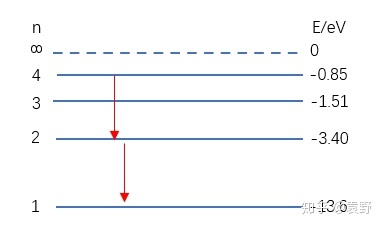 第三种情况,如上图,从第4能级间接跃迁到第2能级,再从第2能级跃迁到第1能级。是以可以放出2种分歧能量的光子 。 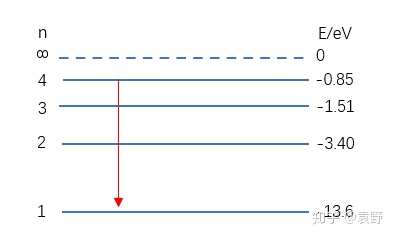 第四种情况,如上图,从第4能级间接跃迁到第1能级。是以只能放出1中能量的光子。 由于只要1个氢原子,上面的四种情况不成能同时发生,是以,最多只能放出3种分歧的光子。 可是有一群氢原子时,情况就纷歧样了,上面的几种情形都能发生,可是分歧的情形中有些光子能量是不异的,总的来说,共能放出6种分歧的光子,以下: 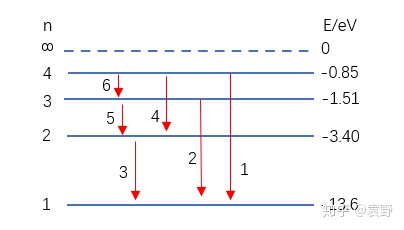 别的,我还对这6种光子的能量巨细停止了排序,如上图所示。 固然这里还有一个公式,小伙们们想记着的就记一下: 一群氢原子处于第n能级的激起态,能够辐射分歧能量的光子为:
【思考2:可见光】对于分歧能级之间跃迁时(高能级向低能级),会发出光子,那末哪些能级之间跃迁会放射出可见光呢? 留意可见光光子的能量范围为1.62eV-3.11eV 经过计较得:当从第n(n=3,4,5,6)跃迁到第2能级时放射出的光子为可见光。 这个小伙伴们可以当做结论记着,今后做题时会节俭很多计较时候! 本期到此竣事了,喜好的小伙伴记得点赞和疯狂扣1哈,不喜好的小伙们请写出 下期再会啦,小伙伴们! |
